РАЗДЕЛ И. ОБЩАЯ ХИМИЯ
3. Химическая связь
Примеры решения типовых задач
Задача 1. Укажите число р-электронов, образующих химические связи в молекуле хлор(И) оксида.
Решение
Сl2O. Строение электронных оболочек элементов Хлора и Кислорода:

Из формулы видно, что Хлор находится в основном (невозбужденном) состоянии и проявляет валентность И. При образовании молекулы оксида происходит перекрытие р-орбиталей двух атомов Хлора ир-орбиталей атома Кислорода:
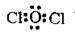
Следовательно, число р-электронов, образующих химические связи в молекуле хлор(И) оксида, равно четырем.
Задача 2. Укажите количество электронов, участвующих в образовании химических связей в молекуле 1,2-дихлоретену.
Решение
Структурная формула вещества:
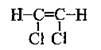
Из формулы видно, что в молекуле есть 6 общих пар электронов. Следовательно, количество электронов, образующих химические связи в молекуле 1,2-дихлоретену, равна 12.
Задача 3. Укажите неметаллические элементы, между атомами которых образование химических связей происходит по схеме:
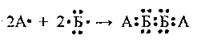
Решение
Элемент А во внешнем электронном слое содержит только 1 электрон - это Водород. Элемент Бы во внешнем электронном слое содержит 6 электронов - это Кислород. Следовательно, это вещество гидроген пероксид.
Задача 4. Укажите тип связи для вещества, образованная элементами с порядковыми номерами 20 и 9.
Решение
Элемент с порядковым номером 20 - Кальций - типичный металлический элемент, щелочноземельный. Элемент с порядковым номером 9 - Фтора - типичный неметаллические элемент, галоген. При их соединении образуется вещество с ионным типом связи.
Задача 5. Элемент А с конфигурацией внешнего электронного слоя 2s22р4 образует ковалентну соединение с Гідрогеном и элементом Б с конфигурацией внешнего электронного слоя 2s22р2 в его возбужденном состоянии. Составьте электронную формулу соединения и укажите общее число электронов, которые приняли участие в образовании связей.
Решение
Элемент А 2s22р4 - Азот, элемент Б 2s22р2 - Карбон. Электронная оболочка Углерода в возбужденном состоянии - 2s12р3. Электронная формула соединения, которая образовалась:
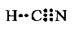
В образовании связи приняло участие 8 электронов.
Задача 6. Из предложенного ряда формул веществ: СО2, SО2, SiО2, LiOH, HF, CuO, C3H8, C6H12O6 выберите такие, которые имеют молекулярные кристаллические решетки. Укажите сумму молярных масс этих веществ.
Решение
Молекулярные кристаллические решетки среди приведенного ряда веществ имеют:
• карбон(ИV) оксид, СO2 - газ (при н. у.), М(СO2) = 44 г/моль;
• сульфур(ИV) оксид, SO2 - газ, M(SO2) = 64 г/моль;
• пропан С3Н8 - газ, М(С3Н8) = 44 г/моль;
• глюкоза С6Н12O6 - твердое вещество, М(С6Н12О6) = 180 г/моль.
Сумма их молярных масс составляет 332 г/моль.