Гальванические элементы. Аккумуляторы
Самые первые источники тока получили свое название в честь итальянского физика Луиджи Гальвани. Примером гальванического элемента может быть элемент конструкции итальянского физика Алессандро Вольты (1799 г.).
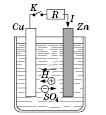
Медная и цинковая пластинки погружены в водный раствор серной кислоты
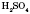
. Цинк и медь растворяются в кислоте. В результате химических процессов медь становится положительным электродом (заряженным положительно относительно цинка), а цинк - отрицательным. Через внешний проводник
R идет ток замыкания ключа
К (за направление тока принят направление движения зарядов от положительного электрода к отрицательному).
 Гальванические элементы
Гальванические элементы - это источники тока с невозобновляемых запасом электрической энергии (например, батарейки для калькуляторов, часов, фонариков и др.).
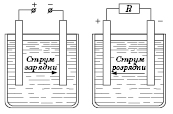
Позже было изобретено источника тока, энергию которых можно восстанавливать, -
аккумуляторы (от лат. «собиратель»). Примером аккумулятора может быть свинцово-кислотный аккумулятор. Если бы в водный раствор серной кислоты погрузили два одинаковые электроды, покрытые оксидом свинца, то они за счет химического растворения свинца в кислоте имели бы одинаковую электрическую полярность (негативную). Аккумулятор сначала заряжают от источника постоянного тока. В результате электролиза на электроде, соединенном с положительным полюсом источника зарядки, выделяется Кислород, а на соединенном с отрицательным полюсом - Водород. Первый из них вызывает дополнительное окисления материала электрода, второй - реакцию восстановления металлического свинца из его оксида. Вследствие этого аккумулятор оказывается заряженным. Направление тока разрядки через проводник
R противоположную направлению тока зарядки, а полярность электродов аккумулятора неизменна.