ЧАСТЬ II
ЗАДАНИЯ ДЛЯ ПРОВЕРКИ ЗНАНИЙ
НЕОРГАНИЧЕСКАЯ
ХИМИЯ
Тема
24. Сульфур
Среди четырех приведенных вариантов
ответов выберите один правильный
1. Выберите свойства, характерные для сероводорода:
A.
Окислительные;
Б. Восстановительные;
B.
Окислительные и восстановительные;
Г. Основные.
2. Укажите
вещество, которое можно использовать для обнаружения сульфат-ионов в растворе:
A. Барий хлорид;
Б. Аргентум хлорид;
B.
Купрум(ІІ) гидроксид;
Г. Магний гидроксид.

3. В
говорите формулу пирита:
A.
FеS2;
Б. FеS;
B.
FеSO4;
Г. Fе2(SO4)3.
4. Укажите
степень окисления Серы в соединении, которое образуется при сгорании сероводорода в
избытке кислорода:
A. +4;
Б. +6;
B. 0;
Г. -2.
5. Укажите
степень окисления Серы в соединении, которое образуется при взаимодействии сульфур(ИV) оксида с кислородом в присутствии
катализатора:
A. +4;
Б. +6;
B. 0;
Г. -2.
6. Отметьте
алотропну модификацию, созданную Сульфуром, которая наиболее стабильна при обычных
условий:
A. Моноклінна сера;
Б. Пластическая сера;
B. Газувата сера;
Г. Ромбическая сера.

Обозначьте порядок цифр, соответствующих
правильным утверждением или ответам
7. Отметьте
схемы превращений, в которых Сульфур проявляет свойства восстановителя:
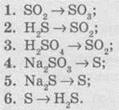
Варианты ответов:
A. 1, 2, 5;
Б. 2, 4, 6;
B. 3, 4, 6;
Г. 1, 3, 5.

8. Отметьте
пары веществ, при взаимодействии которых между собой образуется сульфур(ИV) оксид:
1. SO2 и Н2O;
2. Nа2SO3 и НСl;
3. ГbS и Н2O2;
4. Сu и Н2SO4(концентрированная);
5. Мg и Н2SO4(разведена);
6. Н2S и O2.
Варианты ответов:
A. 1, 2, 5;
Б. 2, 4, 6;
B. 3, 4, 6;
Г. 1, 3, 5.

Установите логическую соответствие между
понятиями в первом и втором столбиках
9. Установите
соответствие между названием вещества и его химической формулой:
Название вещества
1.
Натрий сульфид;
2.
Натрий сульфит;
3.
Натрий сульфат;
4. Натрий тиосульфат.
Химическая формула
A. Nа2SO4;
Б. Nа2S2O3;
B. Nа2S2O7;
Г. Nа2S;
Д. Nа2SO3.

10. Установите соответствие между исходными веществами и
продуктами их взаимодействия:
Реагенты
1. Nа2O + SO2;
2. 2NаОН + SO2;
3. 2NаОН + Н2SO3;
4. NаОН
+ SO2.
Продукты реакции
A. Na2SO3
+ 2Н2О;
Б. Na2SO3;
B. NаНSO3;
Г. Na2SO3
+ Н2O;
Д. NаНSO3 + Н2O.

11. Установите формулы веществ в порядке увеличения
степени окисления Серы:
A. S;
Б. Аl2(SO4)3;
B. К2SO3;
Г. Н2S.

После определенных вычислений напишите свою
ответ, округленный до целого числа с помощью цифр в бланк ответов
12. Вычислите массу (в кг) серной кислоты, которую можно добыть,
используя 0,4 т пирита, содержащего 25 % примесей.
Ответ: