РАЗДЕЛ И. ОБЩАЯ ХИМИЯ
2. Строение атома
2.4. Электрон. Электронные слои
Современная теория электронного строения атома основывается на важном разделе физики - квантовой механике, который описывает свойства микроскопических объектов.
Согласно представлениям квантовой механики, электрон как микрочастица имеет двойственную природу: проявляет свойства частицы и волны. Рассматривается траектория его движения, а лишь вероятность нахождения в пространстве вокруг ядра. Пространство вокруг ядра, в котором вероятнее всего (~90 %) находится электрон, называют орбіталлю. Каждый электрон в атоме занимает определенную орбиталь и образует электронное облако. Электронное облако - это совокупность различных положений электрона, который находится в постоянном движении.
Графически орбитали изображают в виде ячейки, которую также называют квантовой ячейкой  а электроны, которые размещаются на орбитали, показывают стрелками. На каждой орбитали может находиться один или (максимально) два электрона с различными квантовыми характеристиками - спинами1 (принцип запрета Паули).
а электроны, которые размещаются на орбитали, показывают стрелками. На каждой орбитали может находиться один или (максимально) два электрона с различными квантовыми характеристиками - спинами1 (принцип запрета Паули).
Эти два электрона, имеющие противоположные спіни, обозначают в ячейке противоположно направленными стрелками  Такие электроны называют спаренными. Если на орбитали находится один электрон, то его называют неспаренным и обозначают
Такие электроны называют спаренными. Если на орбитали находится один электрон, то его называют неспаренным и обозначают 
Важнейшей характеристикой электрона (при рассматривании его свойств в химии) есть энергия. Электроны, которые имеют одинаковую или близкую по уровню энергию, движутся по близким по размерам орбиталях, образуют энергетические уровни (электронные слои, электронные оболочки). их нумеруют, начиная от ядра: 1, 2, 3, 4, 5, 6, 7 (иногда их обозначат латинскими буквами соответственно К, L, М, N, О, Р, Q). Максимальное количество энергетических уровней элемента численно равен номеру периода, в котором он расположен.
Целое число n, обозначающее номер уровня, называют главным квантовым числом. Оно характеризует энергию электронов, занимающих данный энергетический уровень. Наименьшую энергию имеют электроны первого энергетического уровня, ближайшего к ядру. По сравнению с электронами первого уровня электроны следующих уровней характеризуются большим запасом энергии. Соответственно именно электроны внешнего уровня гораздо слабее связаны с ядром.
Максимальное количество электронов на энергетическом уровне равно удвоенному квадрату номера уровня, то есть:
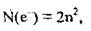
где N(e-) - количество электронов,
n - номер уровня (считая от ядра), или главное квантовое число.
Итак, на первом энергетическом уровне может разместиться не более 2 электронов, на втором - не более 8, на третьем - не больше 18, на четвертом - не более 32.
Максимально заполненный уровень называют завершенным, а электронную оболочку элемента с завершенным внешним энергетическим уровнем - электронной оболочкой благородного газа2.
Энергетические уровни состоят из подуровней. Каждый подуровень также вмещает ограниченное число электронов. Количество подуровней определяется номером энергетического уровня. Число подуровней равно главному квантовому числу: первый уровень имеет один подуровень, второй - два, третий - три, четвертый - четыре подуровня и так далее. Подуровни обозначают латинскими буквами3:
• первый s-подуровень состоит из одной s-орбитали;
• второй р-подуровень состоит из трех p-орбиталей;
• третий d-подуровень состоит из пяти d-орбиталей;
• четвертый f-подуровень содержит семь f-орбиталей.
|
Энергетический уровень
|
Максимальное количество электронов на уровне
|
Подуровни
|
Максимальное число электронов на подуровне
|
|
1
|
2
|
|
2
|
|
2
|
8
|
s
г
|
2
6
|
|
|
|
s
|
2
|
|
3
|
18
|
г
|
6
|
|
|
|
d
|
10
|
|
|
|
S
|
2
|
|
4
|
32
|
г
d
|
6
10
|
|
|
|
f
|
14
|
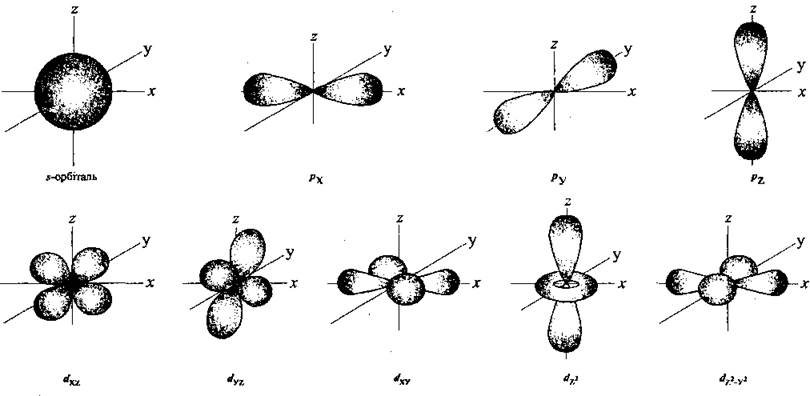
Орбитали находятся на определенных расстояниях от ядра, имеют определенную форму и ориентацию в пространстве. Простейшая форма - сферическая (форма шара). Ее называют s-орбіталлю, а электроны, которые на ней расположены,- s-электронами. Иную форму имеет р-орбиталь: это форма объемной восьмерки или гантели. Такие орбитали расположены в атоме вдоль взаимоперпендикулярных осей пространственных координат 0X, 0Y и 0Z, а поэтому их обозначают рх, ру и рz. В совокупности на трех p-орбиталях максимально может разместиться шесть р-электронов (по два на каждой из них). Существуют и более сложные формы орбиталей:
___________________________________________________________
1 Спин (в переводе с английского - крутиться) характеризует вращение электрона вокруг собственной оси; одно из квантовых чисел (-1/2, +1/2), описывающие свойства элементарных частиц. Квантовые числа в квантовой механике - численные значения квантовых переменных мікрооб'єкта, характеризующих его состояние.
2 Идею стабильности завершенного электронного слоя предложил выдающийся американский физико-химик Джилберт Ньютон Льюис (1875-1946), хотя сам термин октет (октетна теория) он никогда не использовал.
3 Обозначения связаны с начальными буквами слов, что означают представление о возможной форме облаков: s-электронное облако вероятно имеет сферическую форму (фр. sphere), р - гантелеподібну (фр. poignees), d- дископодібну (фр. disque). По современным представлениям d-облако не является дискообразной, следовательно следующие орбитали обозначают буквами латинского алфавита: f, g, h.
2.4.1. Последовательность заполнения орбиталей электронами
Последовательность заполнения электронами орбиталей определяется несколькими принципами. Один из них - принцип минимума энергии: электрон в атоме занимает такое положение, чтобы его энергия была минимальной (правило Клєчковського).
Основное состояние атома характеризуется минимальной энергией. А поэтому электроны заполняют орбитали в порядке увеличения их энергии. Сначала заполняется первый энергетический уровень. Следующий (второй) заполняется только после того, как будет полностью заполнен первый энергетический уровень. Третий заполняется после второго. Электроны, которые размещаются во внешнем энергетическом уровне, называют внешними, или валентными. Именно они определяют химические свойства элементов.
В пределах одного уровня, например второго, сначала заполняется s-подуровень, а затем p-подуровень.
Заметим, что энергия 3d-подуровня выше, чем энергия 4s-подуровня, а поэтому сначала заполняется 4s, а только потом 3d-подуровень и т. д. Распределение энергетических уровней и подуровней в багатоелектронному атоме (в последовательности возрастания энергии): 1s 2s 2р 3s 3р 4s 3d 4р 5s 4d 5p 6s... :
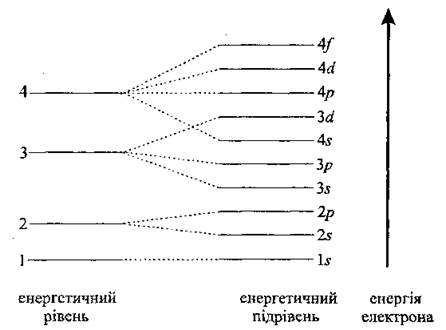
Распределение электронов в атоме по энергетическим уровням и подуровням изображают в виде электронных формул. При составлении электронных формул пользуются следующими правилами:
1. Во время заполнения одного подуровня электроны располагаются так, чтобы суммарный спин был максимальным (это соответствует устойчивому состоянию атома) (правило Гунда).
2. Спіни неспаренных электронов, находящихся на разных орбиталях, должны быть параллельными. Например, если на p-подуровне есть 3 электроны, то их размещают на трех разных орбиталях рх, ру и рz:
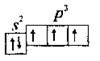
Заполнения электронами уровней и подуровней иллюстрируют электронными формулами и их графическими вариантами. Например, в первом периоде размещено только два элемента - Водород (Н) и Гелий (Не). У Водорода единственный (неспаренный)1 s-электрон на первом уровне, что можно записать так:
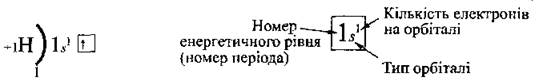
Поскольку на первом уровне может быть не более двух электронов, то у атома Гелия он уже завершен - 2Не 1s2  В атома Гелия на первом энергетическом уровне есть два спаренные s-электроны с противоположными спинами.
В атома Гелия на первом энергетическом уровне есть два спаренные s-электроны с противоположными спинами.
У элементов второго периода заполняется второй энергетический уровень (n = 2). У Лития и Бериллия снова начинает заполняться s-подуровень: 3Li 1s2 2s1 (также записывают сокращенную электронную формулу: 3Li [He]2s1, или 3Li ...2s1, что мы в дальнейшем и будем делать)2, 4Ве [He]2s2. Это тоже s-электроны, но энергия их выше, чем в 1s. Они образуют большие по размеру орбитали, расположенные дальше от ядра.
У следующих шести элементов, начиная от Бора и заканчивая Неоном, заполняется p-подуровень. Электронные формулы этих элементов такие: 5В [He]2s2 2р1; 6Сек [He]2s2 2p2; 7N [He]2s2 2р3;8O [He]2s2 2p4; 9F [He]2s2 2р5; 10Ne [Не]2s2 2р6.
На втором энергетическом уровне, как уже указывалось, может быть не более 8 электронов. У элементов 3-го периода начинает формироваться третий энергетический уровень (n = 3), который максимально может содержать уже 18 электронов; их называют s-элементами (11Na [Ne]3s1; 12Mg [Ne]3s2) и р-элементами (13Al [Ne]3s23p1; 14Si [Ne]3s23p2; 15P [Ne]3s23p3; 16S [Ne]3s23p4; 17Cl[Ne]3s23p5; 18Ar [Ne]3s23p6).
_________________________________________________________________________
1 Количество неспаренных электронов в атоме указывает на возможные значения валентностей элемента. Следовательно, Водород имеет только одну валентность - 1.
2 Под выражением [Не] предусматривают электронную формулу атома последнего из предыдущих благородных газов, в данном случае - Гелия.