ЧАСТЬ И
ОБЩАЯ ХИМИЯ
ОРГАНИЧЕСКАЯ
ХИМИЯ
АРОМАТИЧЕСКИЕ
УГЛЕВОДОРОДЫ (АРЕНЫ)
Химические
свойства аренов
В
связи с тем, что образование ароматического связи (трех сопряженных двойных
связей в шестичленному цикле) является чрезвычайно энергетически выгодным, для аренов
почти не характерны реакции присоединения, несмотря на то, что они являются ненасыщенными
соединениями. Для аренов наиболее характерны реакции замещения. Хотя рядом с
реакциями замещения ароматические углеводороды все-таки могут вступать в реакции
присоединения. Несмотря на то, что эти реакции приводят к нарушению ароматической
системы, они требуют больших затрат энергии и протекают только в жестких
условиях.
1. Галогенування. Бензен и его гомологи
взаимодействуют с хлором или бромом в присутствии катализаторов - безводных АlСl3, Fэвr3 или АlВr3:

С
толуола по этой реакции получается смесь орто - и пара-изомеров.
2. Нитрования. Бензен очень медленно реагирует с
концентрированной нітратною кислотой даже при сильном нагревании. Однако при действии
так называемой нітрувальної смеси (смесь концентрированных азотной и серной
кислот) реакция нитрования проходит достаточно легко:
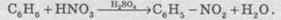
3.
Сульфирование. Реакция легко проходит под действием «дымной» сульфатной кислоты
(олеума):
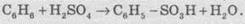
4. Алкилирование по Фриделем-Крафтсом (см. выше
способы получения гомологов бензену).
5. Алкилирование
алкенами. Эти реакции широко используют в промышленности для извлечения
етилбензену и ізопропілбензену (кумола). Алкилирование проводят в присутствии
катализатора АlСl3:
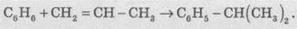
6. Гидрирование
бензену идет при нагревании и высоком давлении в присутствии металлических катализаторов
(Ni, t, Гd). Бензен превращается в циклогексан:
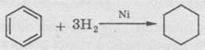
Гомологи
бензену при гидрировании дают производные циклогексана:
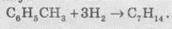
7. Радикальное галогенування бензену происходит
при взаимодействии его паров с хлором только под воздействием жесткого
ультрафиолетового излучения. При этом бензен присоединяет три молекулы хлора
и образуется твердый продукт - гексахлорциклогексан (гексахлоран):
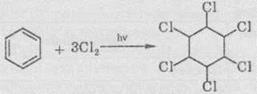
(атомы Водорода в молекуле С6Н6Сl6 не указаны).
8. Реакции в боковой цепи. По химическим
свойствами алкильные радикалы в ароматических соединениях подобные алканов.
Атомы Водорода могут замещаться на галоген, поэтому при отсутствии
катализатора при нагревании или ультрафиолетовом облучении идет радикальная
реакция замещения в боковой цепи. Влияние бензенового кольца на алкильные
заместители приводит к тому, что всегда замещается атом Водорода у атома
Углерода, непосредственно связанного с бензеновим кольцом (α
- атома Углерода).

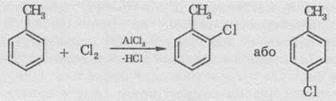
9. Окисления. При действии на гомологи бензену калий
перманганата и других сильных окислителей боковые цепи окисляющиеся. Каким бы
сложным не был цепь заместителя, он разрушается, за исключением а-атома Углерода,
что окисляется в карбоксильну группу. Гомологи бензену с одной боковой цепью
дают бензойную кислоту:
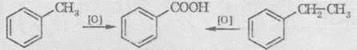
Гомологи,
которые имеют две боковые цепи, дают двохосновні кислоты: