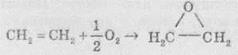ЧАСТЬ И
ОБЩАЯ ХИМИЯ
ОРГАНИЧЕСКАЯ
ХИМИЯ
АЛКЕНЫ
Химические свойства алкенов
Химические
свойства алкенов определяются наличием в их молекуле двойной связи.
При присоединении полярных молекул типа НХ (X; Hаl, ВОН, СN к несимметричных алкенов Водород преимущественно
присоединяется к более гидрогенизированного атома Углерода, примыкающем к
двойной связи (правило Марковникова).
1. Гідрогалогенування. При взаимодействии алкенов с
галогеноводнями (НСl,
НВr) образуются
галогеналкани:
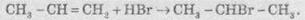
Продукты
реакции определяются правилом Марковникова.
Следует,
однако, подчеркнуть, что в присутствии какого-либо неорганического пероксида
полярные молекулы НХ реагируют с алкенами не по правилу Марковникова:
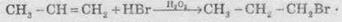
Это
связано с тем, что присутствие пероксида обусловливает радикальный, а не ионный механизм
реакции.
2. Гидратация. При взаимодействии алкенов с водой в
присутствии минеральных кислот (серной, фосфорной) образуются спирты.
Минеральные кислоты выполняют роль катализаторов и является источником протонов.
Присоединение воды идет по правилу Марковникова:
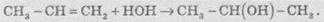
3.
Галогенування. Алкены обесцвечивают бромную воду:

Эта
реакция является качественной на двойную связь.
4.
Гидрирование. Присоединение водорода происходит под действием металлических катализаторов,
чаще всего никеля:

5.
Полимеризация алкенов и их производных:
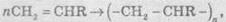
где R = Н, СН3, Сl, С2Н5 и т.д. Молекула СН2 =
СНR называется
мономером, полученная соединение - полимером, число n - степенью полимеризации. Название
полимеров образована от названия мономеров добавлением префикса поле-. Так, с
этилена получают полиэтилен, из пропилена - полипропилен, с хлоретену
(винилхлорида) - поливинилхлорид (ПВХ) и т.д.
6.
Кроме присоединения для алкенов характерны также реакции окисления. При мягком
окислении алкенов водным раствором калий перманганата (реакция Вагнера)
образуются двухатомные спирты:
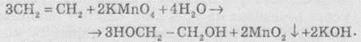
В
результате протекания этой реакции фиолетовый раствор калий перманганата быстро
обесцвечивается и выпадает коричневый осадок манган(ИV) оксида. Эта реакция, как и реакция
обесцвечивание бромной воды является качественной на двойную связь. При жестком окислении
алкенов кипящим раствором калий перманганата в кислой среде происходит
полный разрыв двойной связи с образованием кетонов, карбоновых кислот или СO2,например:

7.
Как и все другие углеводороды, алкены горят и при широком доступе кислорода образуют
карбон диоксид и воду:
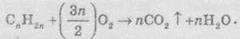
При
ограниченном доступе воздуха горение алкенов может приводить к образованию карбон
монооксида и воды:
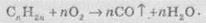
Если
смешать алкен с кислородом и пропустить эту смесь над нагретым до +200 °С серебряным
катализатором, то образуется алкен оксид (епоксиалкан), например: