ЧАСТЬ И
ОБЩАЯ ХИМИЯ
ОРГАНИЧЕСКАЯ
ХИМИЯ
ОБЩАЯ
ХАРАКТЕРИСТИКА ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ
Гибридизация атомов Углерода и геометрия
органических соединений
В
молекулах насыщенных углеводородов существует два типа связей: С-С - ковалентная
неполярная и С-Н - ковалентная слабополярний. Во всех органических соединениях, атомы
Карбона образуют по четыре химические связи. Валентность атома Углерода имеет
оговариваться строением его электронной оболочки. В обычном (основном
состоянии) на внешнем энергетическом уровне атома Углерода находится 4 электрона:
одна пара на орбитали и два неспаренные на р-орбиталях:
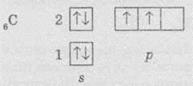
Но
для образования четырех связей на внешнем уровне должно быть четыре неспаренные электроны.
Для этого атом Углерода поглощает небольшое количество энергии и переходит в
возбужденное состояние, в котором строение его электронной оболочки оказывается следующей:
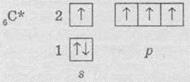
Под
время перехода одного электрона на р-орбиталь орбитали внешнего уровня атома
карбона также меняются: одна s-орбиталь
и три р-орбитали образуют четыре одинаковых по энергии и Форме орбитали:
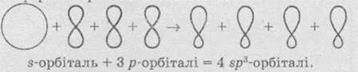
Эти
орбитали называют гібридизованими, а о состоянии самого атома Карбона говорят,
что он находится в состоянии sp3-гибридизации. Поскольку новые орбитали
одинаковые по энергии, они имеют одинаково отталкиваться друг от друга и
поэтому, в отличие от обычных р-орбиталей, которые расположены по
взаимоперпендикулярных осях, sг3-гібридизовані
орбитали в пространстве расположены таким образом, что они направлены к вершинам
тетраэдра (правильной треугольной пирамиды):

При
образовании химических связей атомы Углерода образуют общие электронные пары с
атомами Водорода:
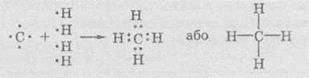
Поскольку
общие электронные пары могут образовываться только при перекрывании орбиталей,
то химические связи образуются в тех же направлениях, в которых направлены
гібридизовані орбитали атома Углерода. Итак, простейший алкан - метан - имеет
форму тетраэдра: атомы Водорода расположены в его вершинах, а атом Углерода -
в его центре:

Сложнее
алканы имеют похожее строение - это комбинация нескольких тетраэдров. Благодаря такой
особенности образования связей в алканах карбоновый цепь не образует линию, а
есть зигзагообразным, причем угол между химическими связями составляет примерно
109,5 °. В молекулах алканов карбоновый скелет может по-разному располагаться
в пространстве благодаря свободному вращению атомов Карбона вокруг одинарных
связей. Например, карбоновый цепь пентана С5Н12 может выглядеть
так:
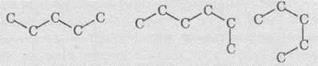
Но
все эти карбоновые скелеты соответствуют одной веществе с неразветвленной цепью:
СН3-СН2-СН2-СН2-CH3.
В
молекулах ненасыщенных углеводородов атомы Углерода также чотиривалентні, но
химические связи они образуют не четырьмя другими атомами, а с меньшим количеством.
Поэтому атомы Карбона также должны быть в определенном состоянии гибридизации.
В
молекуле этилена атомы Углерода соединяются с тремя атомами: два атома
Водорода и один атом Углерода. Для образования такого числа связей атом Карбона
находится в состоянии sг2-гибридизации:
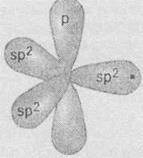
В
таком состоянии у атома Углерода есть три sг2-гібридизовані орбитали, расположенные в одной
плоскости под углом 120° друг к другу. А одна р-орбиталь, что не принимает участия в
гибридизации, расположена перпендикулярно к плоскости гібридизованих орбиталей.
При
образовании химических связей такой атом Углерода с участием гібридизованих
орбиталей образует по одной связи (одной общей электронной паре), с двумя
атомами Водорода и с другим атомом Углерода. А р-орбитали двух соседних атомов
Карбона образуют дополнительную связь:

Таким
образом между двумя атомами Углерода образуются две общие электронные пары:
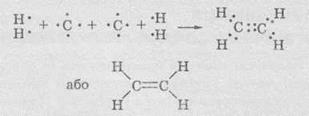
Благодаря
такому расположению орбиталей молекула этилена плоская: все атомы расположены
в одной плоскости, и все валентные углы в ней по 120 °:
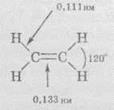
На
отличие от этилена, в ацетилене атомы Углерода находятся в состоянии
8р-гибридизации. В таком состоянии у атома есть только две гібридизовані орбитали,
расположены на одной линии под углом 180 °:
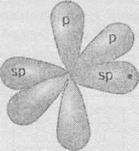
А
две р-орбитали, не участвующие в гибридизации, расположенные взаимно
перпендикулярно к гібридизованих орбиталей. При образовании химических связей в
ацетилене гібридизовані орбитали образуют связи с одним атомом Водорода и
одним атомом Углерода. При этом между атомами Углерода образуется еще два
дополнительные связи с участием негібридизованих р-орбиталей:

Таким
образом между атомами Углерода образуется три общие электронные пары, что соответствует
тройном связи:
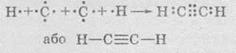
Обратите
внимание, что молекула ацетилена является линейной: все атомы расположены на одной прямой.
И с увеличением кратности связи уменьшается его длина: если в алканах
длина связи С-С составляет 0,154 нм, в алкенах связь С=С имеет длину 0,133
нм, то в ацетилене тройная связь уже 0,121 нм.