ОРГАНИЧЕСКИЕ СОЕДИНЕНИЯ
ЕЩЕ РАЗ О КАРБОН
Сравним электронное строение атомов
Карбона и его соседей по 2-ому периоду. Электроны в атомах этих элементов
располагаются на двух энергетических уровнях. Первый уровень всех атомов
одинаковый, его формула 1s2. Отличается второй уровень:
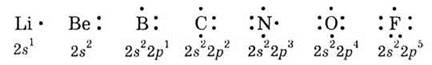
На этом уровне есть четыре атомные
орбитали (МО), они могут образовать максимально четыре ковалентных связи
(четыре связывающие молекулярные орбитали МО). Но только у Карбона реализуется
эта возможность, потому что на его четырех АО находится четыре электроны - по
одному на каждую АО.
Это становится очевидным при рассмотрении
соединений с Гідрогеном элементов 2-ого периода:
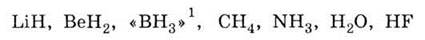
Сравним Карбон с элементами его
группы (IVA). За одинакового строения внешнего,
валентного электронного уровня отличается размер атомов: он увеличивается
сверху вниз в группе.
Атом Карбона - самый маленький атом в
группе. Это означает, что он имеет наибольшую электронную плотность на валентных
орбиталях. Итак, образует прочные химические связи.
Этим определяется уникальность
элемента Карбона: атом с наивысшей валентностью среди самых маленьких атомов (элементов
2-ого периода): самый маленький атом среди атомов с максимальной валентностью
(химических элементов IVA
группы).
Четыре связки, которые может образовать
атом Карбона, предопределяют еще одну очень важную особенность, возможно,
решающую: разнообразие его соединений.
Атомы Углерода, соединенные между собой,
образуют сложные, красивые пространственные структуры в органических соединениях.
_____________________________________________________
1 на самом Деле соединения
ВН3 - борану не существует, поэтому формула записана в кавычках. Простейшая
соединение Водорода с бором В2Н6 - диборан.